Alkalické kovy
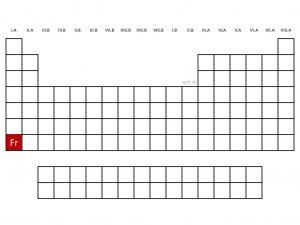
Medzi alkalické kovy zaraďujeme prvky I.A skupiny, okrem vodíka – lítium, sodík, draslík, rubídium, cézium a francium. Tieto prvky sú veľmi reaktívne, čo spôsobuje nízky počet elektrónov na ich valenčných vrstvách – majú iba jeden. Ten veľmi ľahko strácajú a tvoria katióny – ich oxidačné číslo v zlúčeninách je výhradne I.
Vlastnosti alkalických kovov
Sú to mäkké, striebrolesklé kovy, ktoré tvoria bezfarebné soli. Na vzduchu ľahko oxidujú, preto sa uchovávajú v inertnom rozpúšťadle, napr. petroleji. Alkalické kovy veľmi dobre vedú elektrický prúd a teplo. Za vzniku vodíka reagujú s kyselinami.
Ich chemické vlastnosti sú viazané na postavenie jednotlivých prvkov v elektrochemickom rade napätia kovov.
Všetky alkalické kovy prudko reagujú s vodou za vzniku plameňa charakteristickej farby.
Zafarbenie plameňa je špecifické, pre každý z prvkov iné:
lítium – červeno-ružový plameň
sodík – zeleno-žltý plameň
draslík, rubídium, cézium – fialový plameň
Počas tejto reakcie vznikajú alkálie – zásady. Alkalické kovy vytesňujú z vody vodík a vznikajú hydroxidy. Počas reakcie sa uvoľňujú bublinky plynu.
Príklad: pri reakcii draslíka s vodou vzniká hydroxid draselný a vodík.
Popis jednotlivých prvkov alkalických kovov
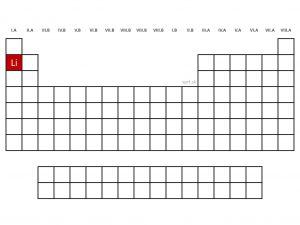
Lítium - Li (Lithium)
Lítium najmenej reaktívnym prvkom spomedzi alkalických kovov. V periodickej tabuľke sa nachádza najvyššie a reaktivita vzrastá s narastajúcim protónovým číslom. Naopak, má najväčšiu elektronegativitu. Pláva na vode, pretože má najnižšiu hustotu spomedzi kovov. Vyskytuje sa najmä vo forme kremičitanov.
Využíva sa v jadrovej energetike, batériách a akumulátoroch, takisto vo farmaceutickom priemysle vo forme organických solí a v leteckom priemysle.
Sodík - Na (Natrium)
Sodík je najbežnejší alkalický kov, vyskytuje sa v množstve minerálov a hornín, napríklad kamenná (kuchynská) soľ, alebo vo forme kremičitanov. Zaraďujeme ho tiež medzi biogénne prvky, má význam v metabolizme buniek. Jeho katión má veľký význam pri udržovaní osmotického tlaku.
Rovnako ako lítium, využíva sa v jadrovej energetike. Je dobrým redukčným činidlom, uplatnenie nachádza aj v sodíkových výbojkách a hasiacich prístrojoch.
Tieto prvky sa často vyskytujú v morskej vode, soľných jazerách, alebo minerálnych vodách. Vyrábajú sa redukciou zo zlúčenín, alebo v prípade Li a Na aj elektrolýzou.
Vytvárajú niekoľko typov zlúčenín. Patria medzi ne hydroxidy, halogenidy, uhličitany a sírany.
Hydroxidy alkalických kovov
Hydroxidy alkalických kovov sú bezfarebné leptavé látky rozpustné vo vode. Príkladom sú hydroxid sodný (NaOH) a hydroxid draselný (KOH).
Sú to silné zásady s hygroskopickými vlastnosťami (pohlcujú vzdušnú vlhkosť).
Sú žieravé a leptavé, využívajú sa na výrobu celulózy, mydla a syntetického hodvábu.
Hydroxid lítny (LiOH) je taktiež hygroskopický, okrem vzdušnej vlhkosti však pohlcuje aj oxid uhličitý. Využíva sa v ponorkách.
Halogenidy alkalických kovov
Halogenidy alkalických kovov sú bezfarebné kryštalické látky s vlastnosťami iónových zlúčenín. Ich vznik popisujeme všeobecnou rovnicou MOH + HX, vzniká MX + voda.
M je všeobecné označenie pre kov, X značí halogén.
Uhličitany alkalických kovov
Uhličitany alkalických kovov pohlcujú vodu – s výnimkou uhličitanu lítneho.
Patria sem látky ako sóda (uhličitan sodný-Na2Co3), aj sóda bikarbóna (hydrogénuhličitan sodný – NaHCO3).
Sóda sa používa na výrobu skla, papiera a mydla, zmäkčovanie vody, aj ako pH regulátor pri fotografických procesoch.
Sódu bikarbónu poznáme ako kypriaci prášok pri pečení koláčov, ale slúži tiež na neutralizáciu žalúdočných kyselín a ako náplň do hasiacich prístrojov.
Zdroje:
BELANOVÁ a spol. 2013. Školská encyklopédia biológie, chémie a fyziky. Bratislava. PRÍRODA
DVOŘÁČKOVÁ. 2013. Chemie pro každého. Olomouc. Rubico
CHRENČÍKOVÁ a spol. 2002. Zmaturuj z chémie. Brno. DIDAKTIS